
想象一下,如果你或你的家人出现了记忆力衰退、行为异常的症状,医生可能会根据临床表现诊断为阿尔茨海默病(老年痴呆),并开具相应的药物。然而,药吃了一堆,病情却毫无起色,甚至持续恶化。这并非医术不精,而是因为我们要面对的敌人,是一个看不见、摸不着的“伪装大师”。
在大脑的微观战场上,除了我们熟知的淀粉样蛋白(Aβ)和Tau蛋白外,还有一个隐藏极深的“杀手”——TDP-43蛋白。它不仅是97%的肌萎缩侧索硬化症(ALS,即“渐冻人症”)的罪魁祸首,还是约45%的额颞叶痴呆(FTD)的主要诱因。更可怕的是,它还会引发一种名为LATE的老年脑病,其症状与阿尔茨海默病惊人地相似,导致大量患者被误诊。
痛点在于:我们至今无法在活人身上“看见”它。
目前的医疗手段,只有在患者去世后进行尸检,才能确认TDP-43病理的存在。这就像是在抓捕罪犯,却只能在案发几十年后通过现场照片来确认凶手,对于当下的治疗和药物研发来说,实在是太晚了。
但是,这一困局即将被打破。一项发表在权威期刊《Nature Communications》上的重磅研究宣布:科学家们成功开发出了全球首创的TDP-43 PET示踪剂——[18F]ACI-19626。这就像是给医生配备了一副“透视眼镜”,终于能让我们在活体大脑中精准定位这个潜伏已久的元凶。
简单来说,TDP-43本来是细胞核里的一个“好人”,负责调节DNA和RNA。但在疾病状态下,它会“离家出走”,跑到细胞质里,并且像滚雪球一样聚集成有毒的团块。这些团块会堵塞神经元的交通,最终导致神经元死亡。
长期以来,神经退行性疾病的诊断严重依赖于对Aβ和Tau蛋白的检测(因为已经有了相应的显影剂)。但TDP-43就像是一个隐形人,现有的技术手段对它束手无策。这就导致了一个巨大的盲区:
为了解决这个问题,研究人员开发了两种小分子放射性药物:ACI-19278和ACI-19626。它们的原理类似于“靶向导弹”,进入大脑后,会特异性地结合到TDP-43的异常聚集体上,并释放出可以通过PET(正电子发射断层扫描)机器捕捉的信号。
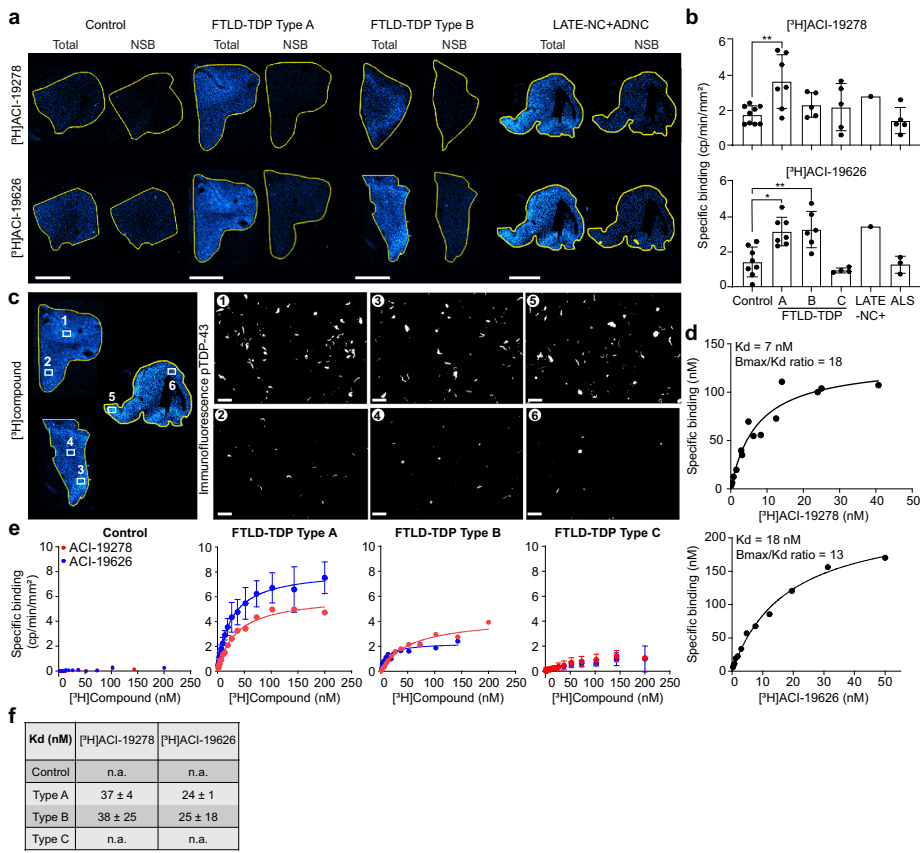
研究团队首先在已故患者的脑组织切片上进行了验证。结果令人振奋:这两种示踪剂不仅能结合,而且结合得非常紧密。
如图[1]所示,这是在不同类型痴呆症患者脑切片上的实验结果。请注意看那些被黄色线条圈出的区域(脑组织切片),在FTLD-TDP(额颞叶变性)Type A和Type B以及LATE-NC患者的样本中,亮蓝色的信号极其强烈,这意味着示踪剂成功地“抓”住了病理蛋白。而在健康对照组(Control)中,信号则非常微弱。这直观地证明了:这个显影剂真的能“照亮”病灶。
更进一步,研究人员利用高分辨率技术,将视角缩小到细胞层面(见图[2])。
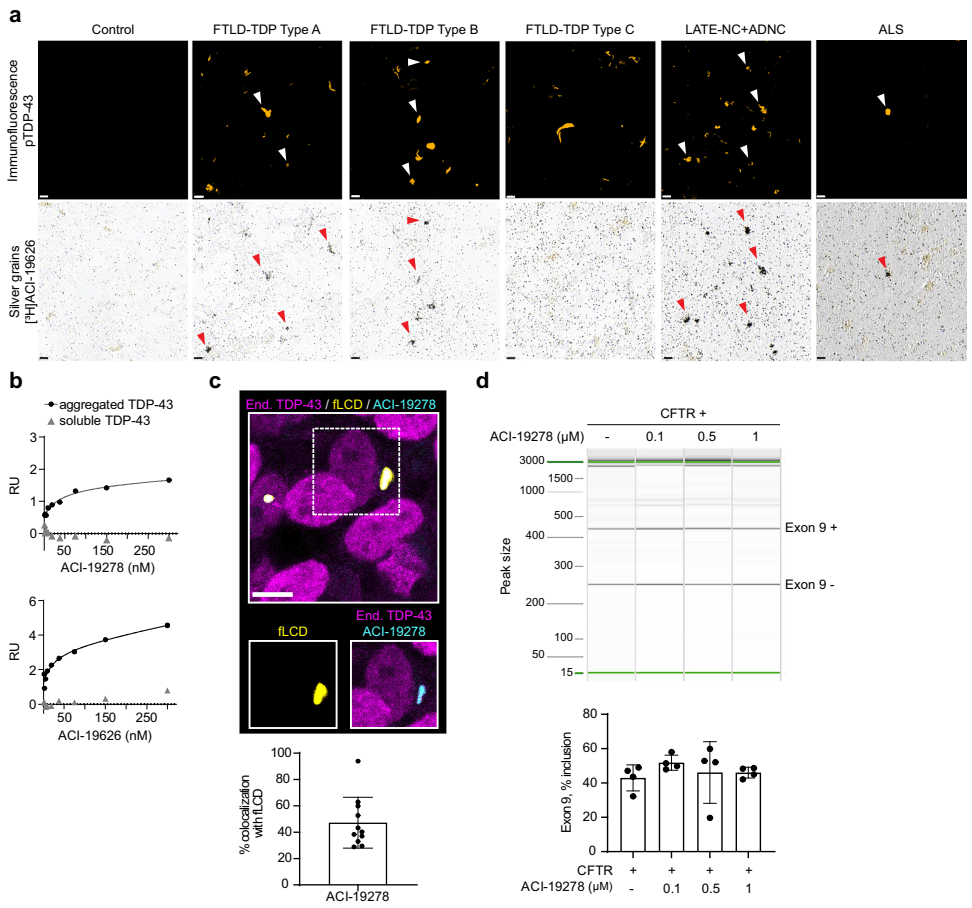
如图[2]所示,上面一排是免疫荧光染色,黄色箭头指的是用抗体标记出的TDP-43病理团块;下面一排是ACI-19626示踪剂的成像,红色箭头指的是示踪剂留下的黑色银颗粒信号。可以清晰地看到,黑色的银颗粒精准地落在了黄色的病理团块位置上。这就像是狙击手精准命中了靶心,实现了对单个细胞内病理沉积的“点对点”锁定。
大脑里的环境非常复杂,尤其是老年人的大脑,往往同时存在多种“垃圾蛋白”。最常见的就是阿尔茨海默病标志性的淀粉样蛋白(Aβ)斑块和Tau蛋白缠结。如果我们的TDP-43“神探”是个脸盲,把Aβ或Tau当成了抓捕对象,那就会导致严重的误诊——这在医学上被称为“脱靶效应”。
为了验证这一点,科学家们特意挑选了患有典型阿尔茨海默病(AD)的脑片进行测试。这些脑片里塞满了Aβ和Tau,但没有TDP-43。结果显示,ACI-19626对这些常见的干扰项视而不见,完全没有产生结合信号。这说明它非常“专一”。
更令人惊叹的是其在混合病理样本中的分辨能力。很多高龄患者(特别是LATE病患者)脑中就像一个大杂烩,既有TDP-43,又有AD病理。在这种极度复杂的环境下,示踪剂还能分清谁是谁吗?
如图[3]所示,这组实验展示了显影剂在“大杂烩”环境下的分辨能力。我们重点看d组图片:
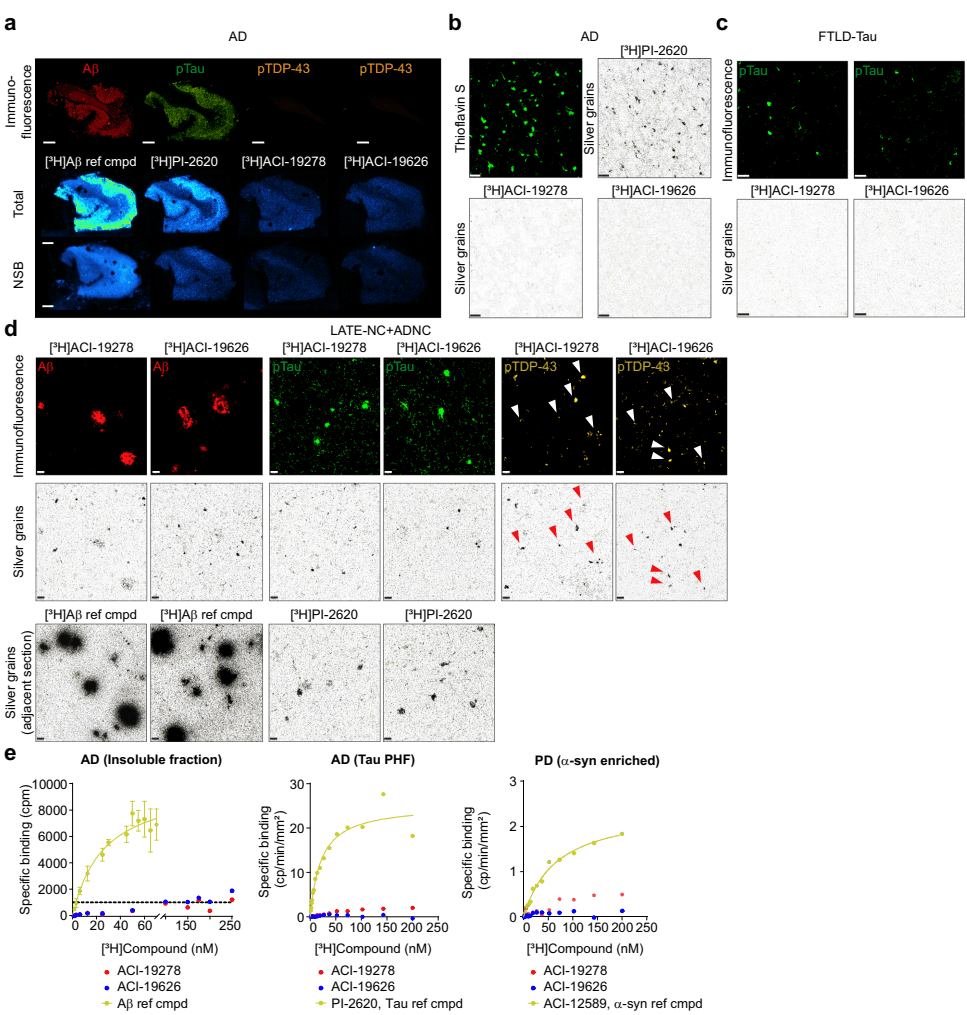
这意味着,即使在满是其他干扰项的“垃圾堆”里,ACI-19626也能临危不乱,精准地揪出那个唯一的“真凶”。这种极高的选择性,是它能够走向临床应用的最核心竞争力。
在培养皿里表现好还不够,药物必须能穿过那道严密的“血脑屏障”,进入活体大脑,并且在完成显影任务后迅速排出,以保证成像清晰且对人体的辐射影响最小。于是,研究团队在恒河猴身上进行了活体PET成像测试。
实验对比了两种候选分子:ACI-19278和ACI-19626。两者都能顺利进入大脑,但在“撤退”的速度上,ACI-19626展现出了决定性的优势。
如图[4]所示,这是恒河猴大脑的PET动态扫描成像图:
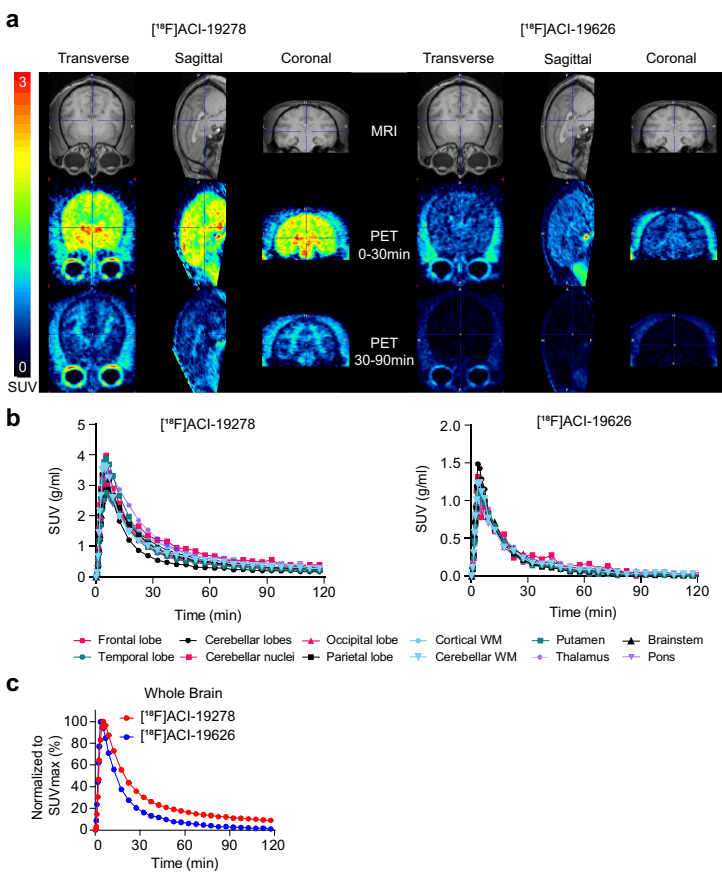
这种“快进快出”的特性极大地提高了信噪比。就像是在黑夜里打手电筒找东西,背景越黑,我们要找的目标(发光的病灶)就越清晰、越显眼。正因如此,ACI-19626击败了同门兄弟,被最终选定为全球首个进入人体临床试验的TDP-43 PET示踪剂。
长期以来,神经退行性疾病的治疗之所以步履维艰,很大程度上是因为我们在“盲人摸象”。把TDP-43病理的患者当成阿尔茨海默病去治,自然是缘木求鱼,这也是导致过去几十年阿尔茨海默病新药研发失败率居高不下的重要原因之一——病人可能一开始就找错了。
[18F]ACI-19626的问世,不仅仅是多了一个诊断工具,它可能彻底改变这一领域的游戏规则:
目前,ACI-19626即将开启首次人体临床试验(First-in-Human)。这是否意味着我们离攻克渐冻症、额颞叶痴呆以及复杂的老年痴呆症又近了一步?当大脑中的迷雾被层层拨开,或许真正的治愈方案,就藏在这些即将被点亮的影像之中。
未来的某一天,当体检单上多了一项“脑部蛋白扫描”,我们或许就能在记忆消失之前,真正守住大脑的防线。
本文由超能文献“资讯AI智能体”基于4000万篇Pubmed文献自主选题与撰写,并经AI核查及编辑团队二次人工审校。内容仅供学术交流参考,不代表任何医学建议。
分享
一项涉及1800多份大脑扫描的“超级分析”发现,儿童和成年人强迫症(OCD)的神经生物学基础可能截然相反,颠覆了传统认知。儿童大脑表现出“过度努力”的代偿性激活,而成年人则呈现出“疲软”或“耗竭”的激活减弱。