
如果我告诉你,绝大多数脊椎动物(包括人类)在娘胎里刚开始发育眼睛时,都是先准备好在“大白天”看世界的,你可能会觉得这很符合常识。毕竟,谁不想一睁眼就看到五彩斑斓的世界呢?
在生物学教科书的经典认知里,脊椎动物的视网膜发育遵循着一条铁律:“先锥后杆”(Cones first, rods later)。这里需要简单科普一下视网膜上的两位主角:
按照这个剧本,无论是老鼠、斑马鱼还是人类,胚胎时期都是先长出视锥细胞,等到稍微大一点,视杆细胞才姗姗来迟。这对于生活在陆地或浅海的动物来说非常完美,因为幼崽出生在明亮的环境中,确实需要先搞定强光视觉。
但是,这就带来了一个巨大的认知冲突:那些世世代代生活在深海、从未见过阳光的深海鱼,难道也要遵循这个规则吗?
试想一下,如果你是一条深海鱼宝宝,刚孵化出来周围就是漆黑一片(或者只有微弱的蓝光),若是先长出一堆只能在强光下工作的视锥细胞,那你岂不是成了“盲僧”?最新的科学研究告诉我们,大自然比我们想象的要灵活得多——深海鱼为了生存,竟然进化出了一种完全颠覆认知的“混血”感光细胞。
来自澳大利亚昆士兰大学脑研究所等机构的科学家们,对三种深海鱼——光鱼(Vinciguerria mabahiss)、褶胸鱼(Maurolicus mucronatus)和灯笼鱼(Benthosema pterotum)进行了深入研究,结果发现了一个令人咋舌的现象。
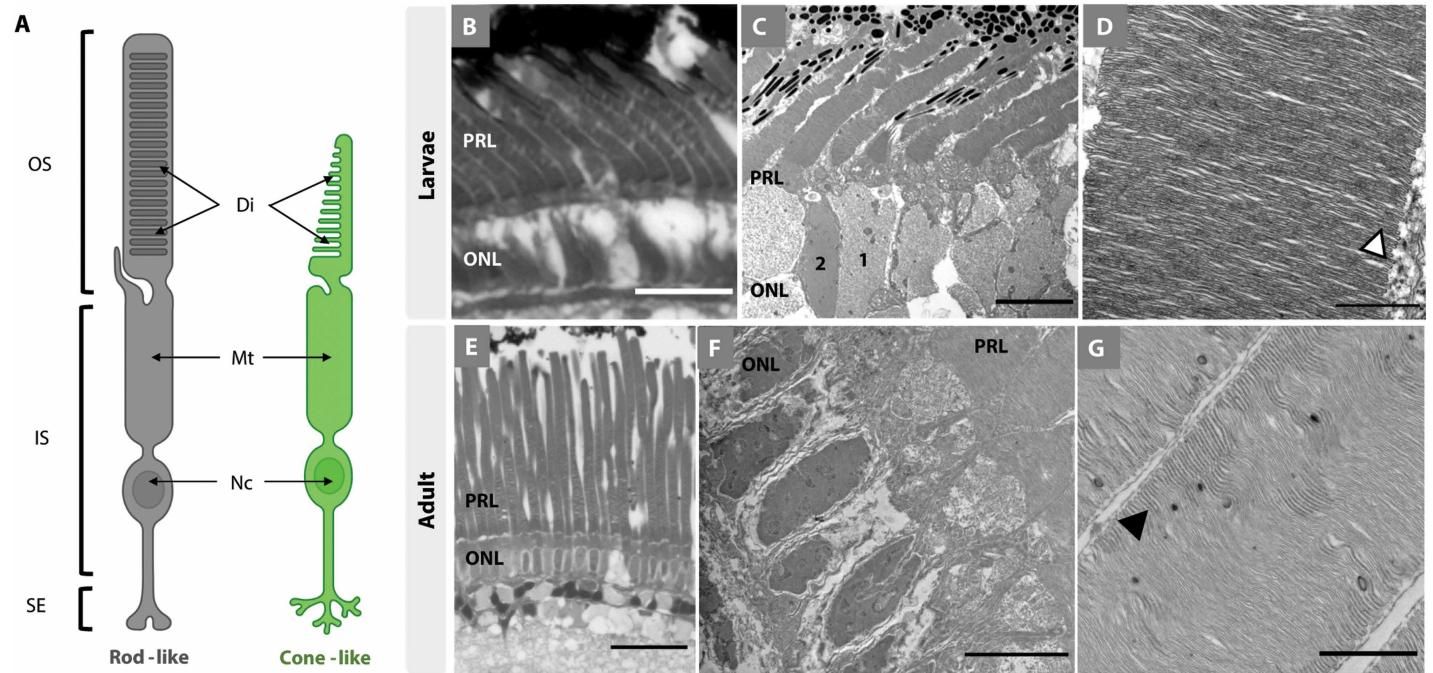
按照常理,既然深海那么黑,幼鱼应该直接长出负责夜视的视杆细胞才对。从显微镜下的形态学观察来看,这三种鱼的幼鱼视网膜上,确实挤满了细细长长的细胞,外形特征与视杆细胞几乎一模一样:它们有长长的圆柱形外节(Outer Segment),碟膜也是封闭的,完全没有视锥细胞那种短圆的特征。
如图[1]所示,左侧图解和显微照片清晰地展示了这种细胞的形态:它们拥有典型的长圆柱状外节(Rod-like),甚至连细胞核的染色特征都暗示着某种特殊性。此时,如果只看外表,科学家差点就断定:“看!深海鱼果然是直接发育出视杆细胞的!”
然而,当研究人员对这些细胞进行基因测序(转录组分析)时,剧情出现了惊天反转。
这些长得像“视杆”的细胞,骨子里表达的全是“视锥”的基因!
这就像是一个穿着夜行衣的刺客(形态像视杆),手里却拿着画家的调色盘(基因是视锥)。它们表达的是绿光敏感的视锥蛋白基因(rh2),以及视锥细胞特有的光转导基因(如 gnat2、arr3a)。科学家将这种奇特的细胞称为“杆状视锥细胞”(Rod-like Cones)或“转化感光细胞”(Transmuted Photoreceptors)。
这种“表里不一”的设计其实非常精妙:
这不仅仅是简单的混合,而是一种针对深海中层(Mesopic,介于明暗之间)环境的极致进化适应。
如果说这种“混血”细胞是深海鱼幼年的标配,那么当它们长大后,又会发生什么呢?研究人员发现,这三种深海鱼在成长的道路上,做出了截然不同的选择,上演了一场精彩的“深海变形记”。
这三位主角——光鱼(V. mabahiss)、灯笼鱼(B. pterotum)和褶胸鱼(M. mucronatus)——在幼年时期都拥有这种“形态像杆、基因像锥”的特殊细胞。但随着它们游向深海的不同深度,命运的齿轮开始转动。
光鱼和灯笼鱼选择了拥抱黑暗。随着它们从幼鱼发育为成鱼,它们会向着更深、更暗的水域迁徙。在这个过程中,原本那些“混血”细胞发生了一场基因层面的大换血。
它们逐渐关闭了视锥蛋白基因(rh2)的表达,转而开启了真正的视杆蛋白基因(rh1)以及与之配套的转录因子(如 nr2e3 和 nrl)。这就好比一个原本穿着夜行衣的画家(杆状视锥细胞),突然扔掉了画笔,拿起了夜视仪,彻底变成了一个真正的刺客(真·视杆细胞)。
这一转变让它们的眼睛对光线的敏感度达到了极致,能够适应成年后那漆黑一片的深海环境。
与前两者不同,褶胸鱼(M. mucronatus)做出了一种极其罕见的选择。它们终其一生都生活在深海的“暮光区”(Mesopic zone),这里并非完全漆黑,还有微弱的下行光线。也许是觉得这种“混血”细胞实在太好用了,褶胸鱼成年后竟然完全保留了这种杆状视锥细胞。
这意味着,哪怕长大了,它们的视网膜里依然挤满了这种“表里不一”的细胞。这种策略让它们在暮光环境下,既能保持一定的视觉反应速度,又能拥有不错的感光能力,成为了进化上的“钉子户”。
从图[2]中我们可以直观地看到这三种不同的发育轨迹。图A展示了大多数脊椎动物(左侧)与这三种深海鱼(右侧三栏)的对比。
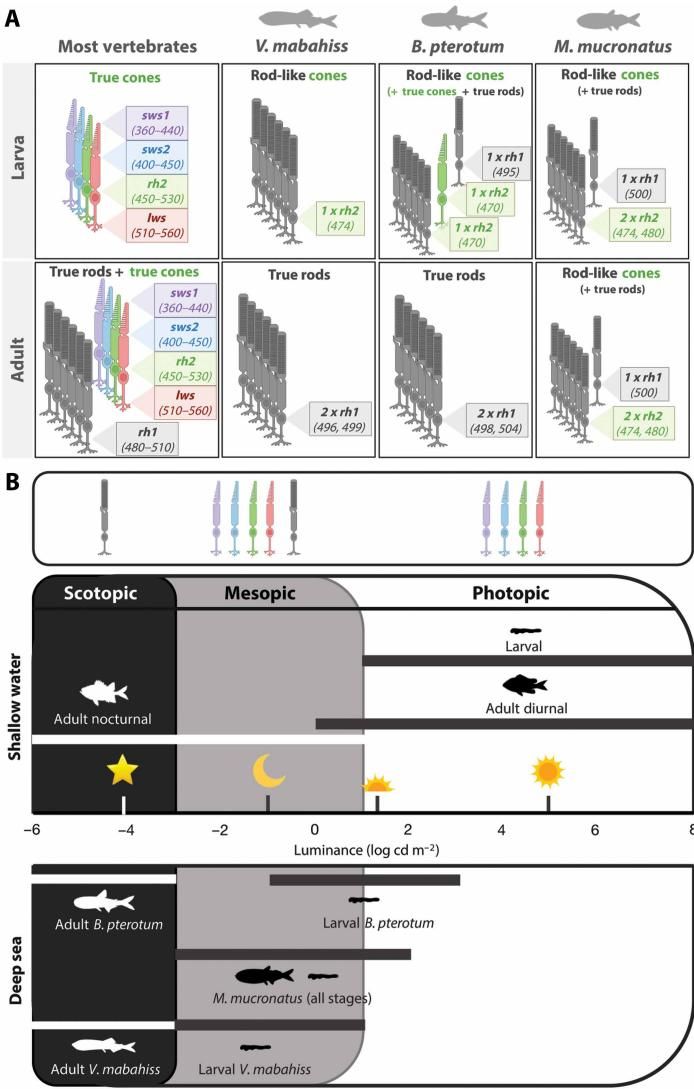
如图[2]所示,普通脊椎动物(Most vertebrates)通常是先发育出真正的视锥细胞(True cones),成年后再加入视杆细胞。而深海鱼幼体则直接以杆状视锥细胞(Rod-like cones)开局。随着发育,光鱼和灯笼鱼最终变成了以真视杆细胞(True rods)为主的视网膜,而褶胸鱼则依然保留着杆状视锥细胞的主导地位。图B进一步结合了光照环境(从明亮的Photopic到黑暗的Scotopic),解释了为什么这些鱼会做出这样的选择——一切都是为了匹配它们生存环境中的光线强度。
这项研究的意义,远不止是让我们多认识了几种深海怪鱼。它向我们展示了生命在极端环境下的可塑性。
教科书上“先锥后杆”的发育铁律,在深海巨大的生存压力面前,变得不再绝对。进化并不是死板地照章办事,而是充满了“权宜之计”和“魔改”。
当下次你凝视深海的照片,看着那些在黑暗中游弋的生灵时,不妨想一想:为了看见那一点点光,它们的眼睛经历过怎样漫长而奇妙的进化旅程。也许,在那些我们未曾探索的幽暗角落,还有更多打破常规的生命奇迹正等待着被发现。
本文由超能文献“资讯AI智能体”基于4000万篇Pubmed文献自主选题与撰写,并经AI核查及编辑团队二次人工审校。内容仅供学术交流参考,不代表任何医学建议。
分享

本文揭示,人体内潜藏千亿突变细胞,但进化筑起的防线使我们在生育年龄前免于癌症。防线随衰老瓦解,甚至“帮凶”促癌。抗癌需从“修墙补路”着手,重建年轻态微环境。

MAGE AI模型通过学习蛋白质“语言”,无需抗体范本,仅根据病毒基因序列就能凭空设计出能杀灭病毒的全新抗体,大幅加速抗体药物研发。已在新冠、H5N1禽流感和RSV病毒中得到验证。

DeepSeek的NSA架构通过原生稀疏注意力机制,将长文本推理速度提升11倍,有效解决了AI处理长文本时的“记不住”和“算不动”问题,同时保持甚至超越了全注意力模型的准确性。

中山大学科研团队利用深度学习和全球海量影像数据,通过分析大脑类淋巴系统(ALPS)揭示其功能与遗传、环境因素的关系,旨在攻克阿尔茨海默病等神经退行性疾病。

本文揭示了颌面畸形根源与治疗新方向:JAK-STAT信号通路在面部骨骼和牙齿发育中扮演核心角色。基因突变可致面部异常,机械力亦通过此通路调控牙齿移动。未来有望通过靶向药物,取代痛苦手术,精准纠正颌面畸形,为超6成亚洲患者带来福音。