
病毒也会“打架”:2009年甲流如何重塑RSV流行周期
在呼吸道病毒的世界里,并非总是“祸不单行”,有时它们也会因争夺宿主而相互排斥。这种现象被称为“病毒干扰”(Viral Interference)。
自COVID-19大流行以来,我们见证了流感、RSV(呼吸道合胞病毒)等呼吸道传染病的消退与反弹,这种剧烈的波动引发了公众对“多重疫情”的担忧。然而,这种病毒间的复杂博弈并非首次上演。近日,发表在权威期刊《Nature Communications》上的一项研究,通过重建斯德哥尔摩长达20年的流行病学历史,揭示了一个引人深思的案例:2009年的H1N1甲型流感大流行,竟凭一己之力彻底改变了RSV的流行节奏,将其原本规律的“大小年”周期推倒重来。
这项由耶鲁大学公共卫生学院与瑞典卡罗林斯卡医学院合作完成的研究,不仅为我们解开了斯德哥尔摩RSV流行模式突变的谜团,更为理解不同呼吸道病毒在种群层面的相互作用提供了坚实的量化证据。
1. 斯德哥尔摩的“生物钟”失灵:从井然有序到突发混沌
RSV是导致婴幼儿和老年人下呼吸道感染的主要元凶之一,在全球温带地区,它通常在冬季爆发。在瑞典斯德哥尔摩北部,RSV的活动曾有着如同精密钟表般的规律——双年周期(Biennial Cycle)。
在该地区,RSV呈现出一种典型的“大小年”交替模式:
- 奇数年(大年):疫情来得早且猛烈(如2001/02雪季)。
- 偶数年(小年):疫情来得晚且温和(如2002/03雪季)。
这种规律在2009年之前一直非常稳定。然而,2009年全球爆发了H1N1甲型流感大流行,随后斯德哥尔摩的RSV监测数据出现了一个令人困惑的异常。
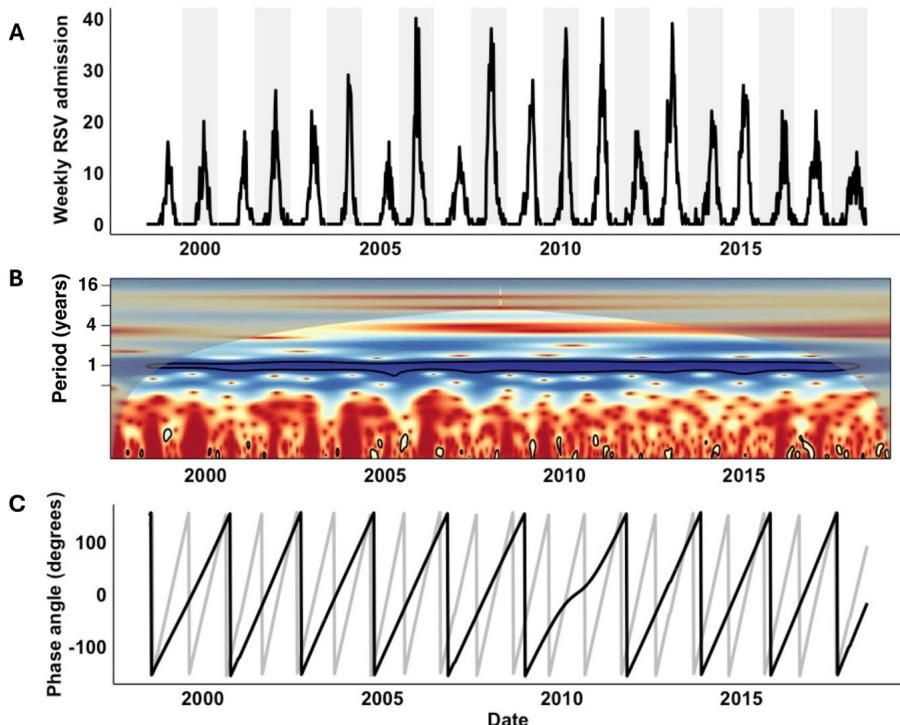
如图[1]所示,长达20年的监测数据显示,RSV的流行节奏在2009年被突然打断。原本应该是一个“大年”的2009/10雪季,疫情却意外地推迟了;紧接着的2010/11雪季本该是“小年”,却爆发了一场大规模疫情。从图[1]C部分的相位角分析中我们可以清晰地看到,黑线代表的双年周期相位在2009年前后发生了剧烈的偏移。这意味着,仅仅一个流感大流行季,就导致RSV的周期发生了“相位漂移”,从此在这个地区,偶数年变成了大爆发的年份,与之前的规律截然相反。
2. 谁动了RSV的“奶酪”?三大嫌疑人的博弈
为了查明导致这一剧变的真凶,研究团队构建了一个分年龄层的机制性传播模型(Age-stratified Mechanistic Model),并提出了三个可能的假设进行逐一排查:
- 嫌疑人A:婴儿潮(出生率激增)。 2010年当地出生率确实增加了10%。新生儿是RSV的主要易感人群,出生率的波动是否足以撼动流行周期?
- 嫌疑人B:严冬(气候因素)。 2009/10和2010/11的冬天异常寒冷。低温和干燥通常有利于呼吸道病毒的存活与传播,这是否是导致连续大爆发的原因?
- 嫌疑人C:病毒霸凌(病毒干扰)。 2009年H1N1流感大流行主要发生在秋季(9月-11月),恰好处于RSV流行季开始之前。是否是流感病毒激发了人群的免疫系统,从而暂时抑制了RSV的传播?
3. 数学模型给出的判决:只有一种解释站得住脚
研究人员利用长达20年的周度住院数据对模型进行了拟合与训练。结果令人惊讶:传统的解释失效了。
当研究人员仅考虑出生率变化或气候因素(气温、湿度)时,模型虽然能重现2009年之前的规律,但完全无法复现2009年之后的周期反转。也就是说,仅靠多生孩子或天气变冷,解释不了为什么RSV的流行节奏会彻底掉个头。
唯有引入“病毒干扰”机制的模型,完美复现了历史数据。如图[2]所示,Model 3(最下方)假设病毒干扰效应在不同时期(大流行前、大流行期间、大流行后)存在差异,其预测曲线(蓝色)与实际观测数据(黑色)展现出了极高的一致性。
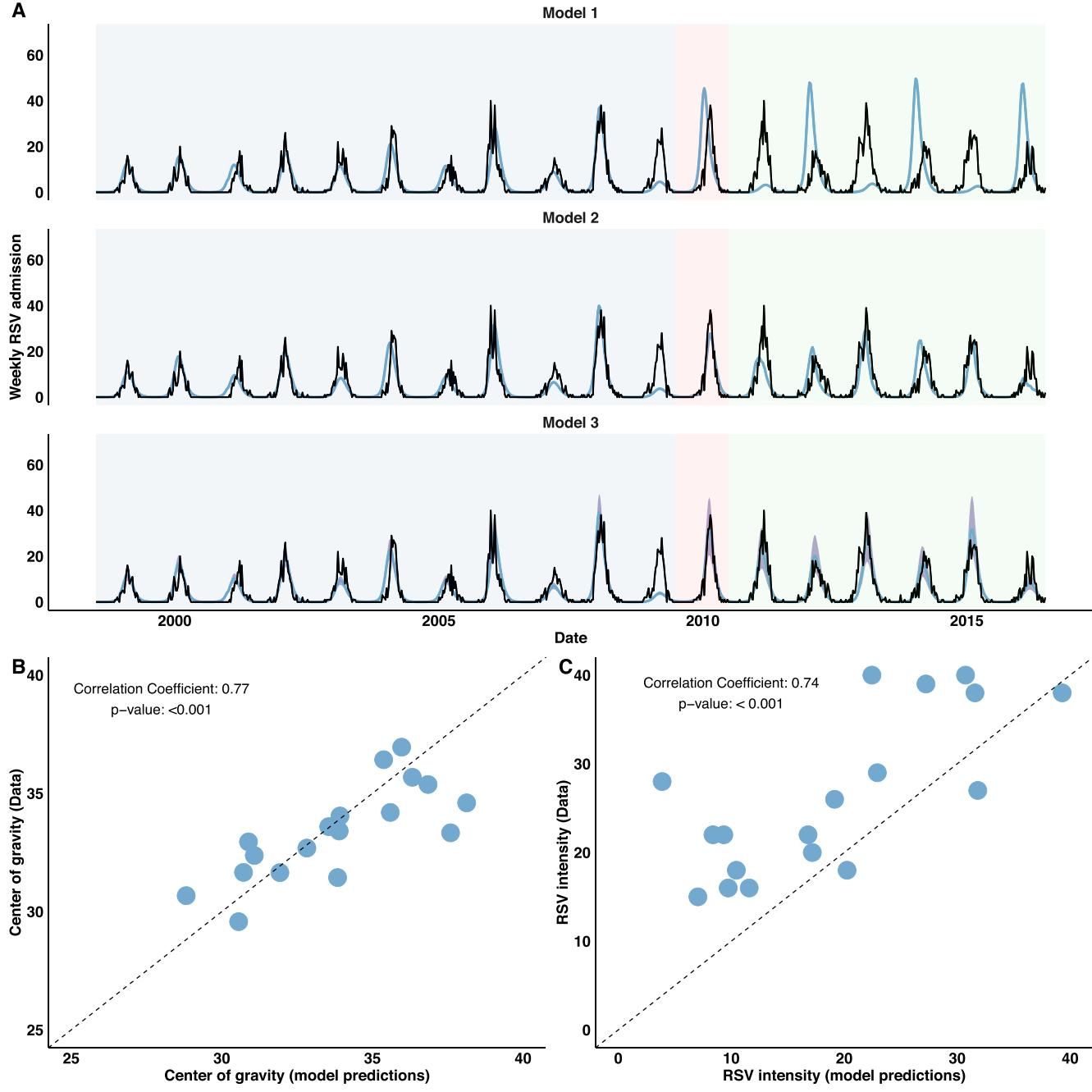
从图[2]中我们可以看到,引入病毒干扰机制后,模型成功预测了2009/10雪季RSV疫情的推迟和规模缩小,同时也精准预测了随之而来的2010/11雪季的反常大爆发。通过对比相关性系数,Model 3在预测疫情重心(Center of gravity, r=0.77)和强度(Intensity, r=0.74)方面均表现优异。这有力地证明,正是2009年H1N1流感的强势介入,通过免疫干扰机制“重塑”了RSV的传播动力学。
4. H1N1的“霸权”:短暂但强效的免疫压制
这项研究最令人着迷的发现之一,是不同流感病毒对RSV的“压制力”存在显著差异。研究团队通过贝叶斯推断方法量化了这种干扰效应,结果显示2009年的H1N1大流行流感毒株表现出了最强的干扰能力。
如图[3]所示,不同颜色的直方图代表了不同时期流感对RSV的干扰强度(取对数坐标)。蓝色区域代表2009年H1N1大流行期间的干扰效应,其中位数估计值高达-1.23,远高于大流行前季节性流感(橙色区域,-2.69)的干扰水平。这意味着H1N1病毒在感染宿主后,能激发一种更为强烈、足以“屏蔽”RSV感染的短期免疫反应。
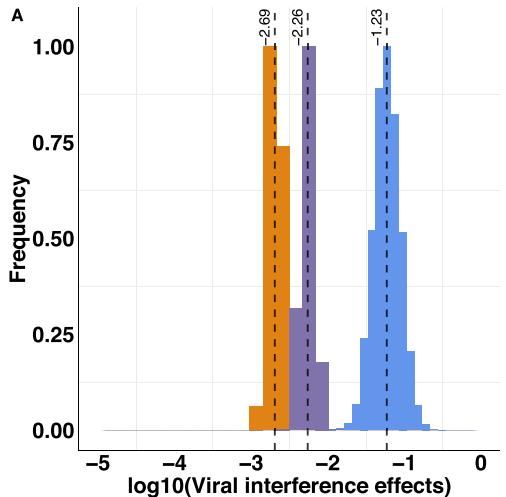
更有趣的是,这种保护作用虽然强劲,却非常短暂。模型估算显示,流感感染带来的针对RSV的暂时性免疫保护(Innate Immunity)平均仅持续约5天(95%置信区间:0.55-19.01天)。这与之前的动物实验结果不谋而合——雪貂实验表明,只有当两次感染间隔在一周以内时,才会出现显著的病毒干扰现象。但这短短几天的“免疫窗口”,放在群体层面,却足以引发一场长达数年的流行病学海啸。
5. 蝴蝶效应:易感人群的“堰塞湖”
为什么一个短期的干扰能导致RSV流行周期发生永久性逆转?答案在于“易感人群”的动态变化。RSV之所以会有周期性爆发,是因为每次大爆发都会大量消耗人群中的易感个体(主要是新生儿和幼儿),随着易感人群耗尽,疫情自然平息,直到新一批婴儿出生补充了“燃料”。
研究人员通过模型还原了这一过程的微观机制,如图[4]所示。图[4]A清晰地展示了易感人群规模随时间的变化轨迹。请注意2009-2010年这一关键节点(粉色阴影区域):
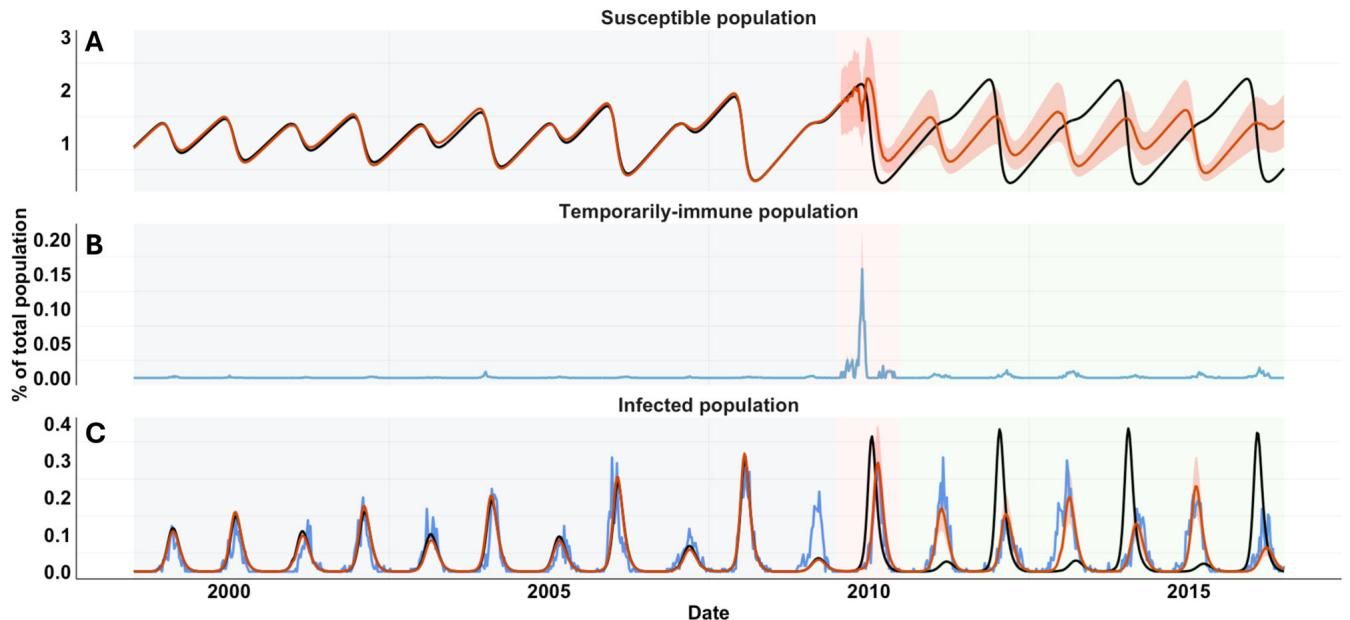
- 黑色曲线(无干扰假设):按照正常节奏,易感人群数量应在冬季随着RSV疫情爆发而迅速下降。
- 红色曲线(有干扰假设):由于H1N1流感的提前爆发,大量儿童先感染了流感,暂时对RSV免疫。这导致原本该被RSV感染的人群“躲过一劫”,易感人群没有被消耗,反而像堰塞湖一样积攒了起来。
这种积压直接导致了随后的2010/11雪季(图[4]C中紧随粉色区域后的高峰),拥有了比往年更充足的“燃料”——易感人群处于高位。于是,一场本该是“小年”的温和疫情,演变成了一场猛烈的大爆发。这次意外的大爆发彻底打乱了原有的消耗-补充节奏,使得RSV的流行周期从此发生了相位翻转。
6. 启示:多病毒共存时代的公共卫生策略
这项研究不仅解开了斯德哥尔摩RSV周期之谜,更为我们理解后疫情时代的传染病趋势提供了重要镜鉴。正如2009年的H1N1重塑了RSV格局,近年来COVID-19大流行期间非药物干预措施(NPIs)的实施与解除,同样在全球范围内引发了RSV和流感的反常反弹。
结论是明确的:呼吸道病毒之间存在着复杂的生态互动。 当我们评估一种病毒的流行风险或制定疫苗接种策略时,不能将其视为孤立事件。一种病毒的爆发或消退,可能会通过免疫干扰或改变易感人群库,在整个生态系统中引发连锁反应。在未来,建立多病原体联合监测预警体系,将是应对不确定的呼吸道传染病威胁的关键。
论文信息
- 标题:Unraveling the role of viral interference in disrupting biennial RSV epidemics in northern Stockholm.
- 论文链接:https://doi.org/10.1038/s41467-025-63654-1
- 论文一键翻译:点击获取中文版 ➡️
- 发表时间:2025-8-30
- 期刊/会议:Nature communications
- 作者:Ke Li, Johan Hamrin, Anna Nilsson, ..., Virginia E Pitzer
本文由超能文献“资讯AI智能体”基于4000万篇Pubmed文献自主选题与撰写,并经AI核查及编辑团队二次人工审校。内容仅供学术交流参考,不代表任何医学建议。
分享



