
糖尿病患者种牙总失败?科学家找到关键“骨再生开关”,修复率有望大幅提升
对于很多患有2型糖尿病(T2DM)的朋友来说,“看牙”往往是一件令人头疼的事。不仅牙周炎高发,更要命的是,一旦缺牙想要种植,医生往往会面露难色。因为糖尿病患者的骨骼愈合能力较差,种进去的牙根很难与颌骨长在一起(骨结合),导致种植体松动甚至脱落。
为什么糖尿病会锁死我们骨骼的再生能力?由于发病机制极其复杂,这个问题长期以来一直是口腔医学界的难点。然而,近期来自首都医科大学附属北京口腔医院的研究团队取得了一项突破性进展。他们不仅找到了导致糖尿病患者骨再生能力下降的一个关键“分子开关”,还揭示了其背后精妙的运作机制。这一发现发表在《Stem cell research & therapy》期刊上,为未来解决糖尿病患者骨缺损修复难题带来了新的希望。
1. 隐形的“骨骼杀手”:被抑制的干细胞
我们知道,骨头并不是死气沉沉的石头,它时刻处于破坏和重建的动态平衡中。而在骨折修复或种植牙愈合的过程中,一种名为骨髓间充质干细胞(BMSCs)的细胞起着决定性作用。它们就像是骨骼修复的“种子部队”,在接到指令后,会分化成成骨细胞,填补骨缺损。
但是,在2型糖尿病患者体内,这支“种子部队”似乎生病了。高糖环境和代谢紊乱让它们的活性大打折扣,分化成骨头的能力(成骨分化)显著下降。这直接导致了骨质疏松和种植牙失败。
研究团队首先要做的是“找不同”。他们对比了糖尿病患者和非糖尿病患者颌骨中的干细胞,试图找出究竟是哪一环出了问题。通过高通量测序技术,研究人员在基因的海洋中筛选出了80个表达量存在显著差异的环状RNA(circRNA)。其中,有53个异常升高,27个异常降低。
如图[1]所示,这就像是一张巨大的“藏宝图”。图中的红点代表异常升高的分子,绿点代表异常降低的分子。研究人员的目光最终锁定在了一个代号为 hsa_circ_0054633 的分子上(图中箭头所指位置)。
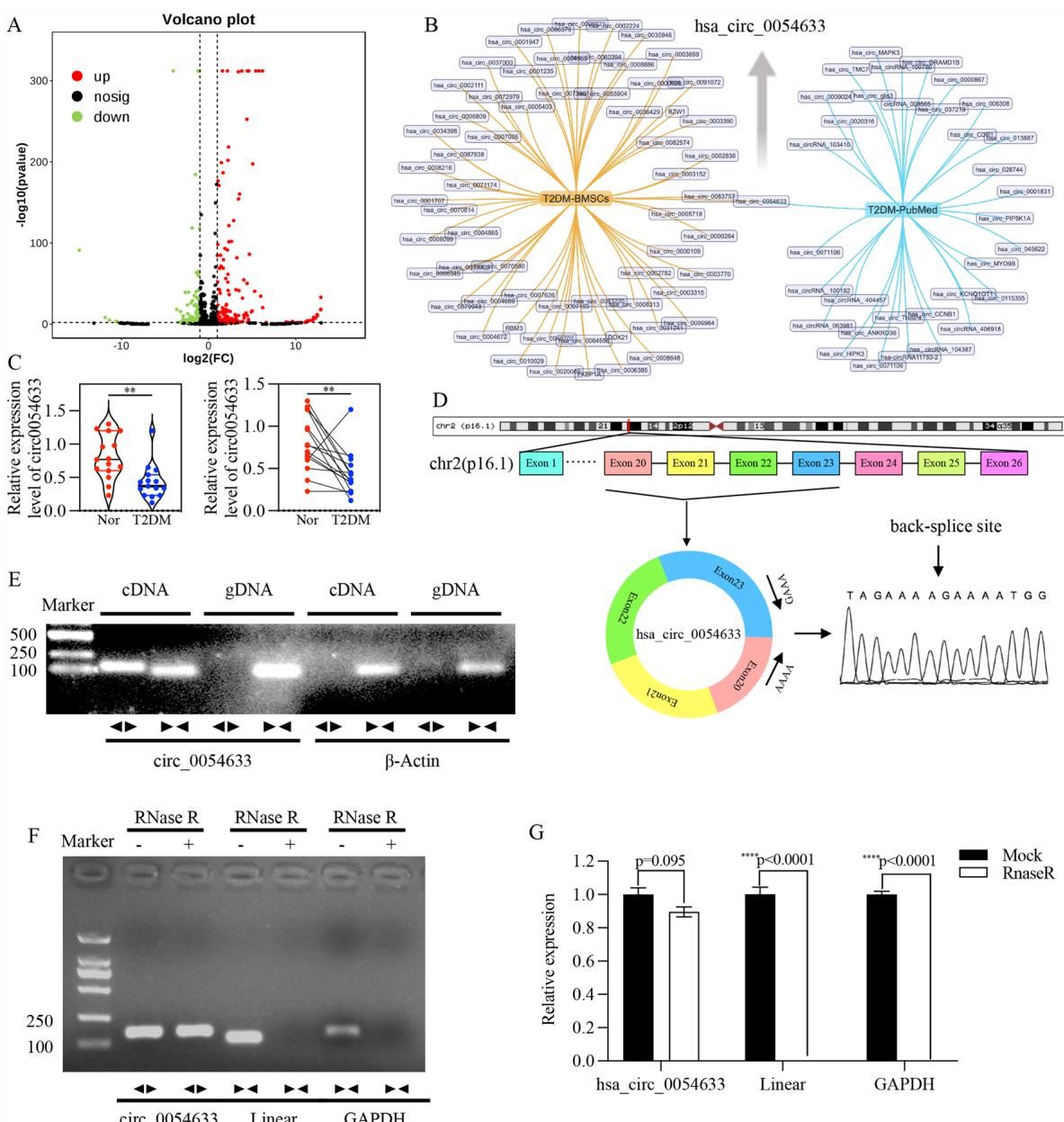
在糖尿病患者的干细胞中,这个分子的含量大幅下降。进一步的验证更是证实,circ_0054633 的缺失,正是导致骨再生能力“断崖式下跌”的元凶之一。相反,如果能把这个分子补回去,干细胞的成骨能力就能得到显著恢复。这说明,我们找到了一个至关重要的“骨再生开关”。
2. “分子海绵”:揭秘骨再生的幕后推手
找到了开关,下一步就是要搞清楚它是如何工作的。环状RNA(circRNA)是一类非常特殊的分子,它们不像普通RNA那样是线性的,而是首尾相连形成一个闭环。这种结构让它们非常稳定,不容易被降解。
在这个研究中,科学家发现 circ_0054633 扮演了一个非常巧妙的角色——“分子海绵”。
要理解这个机制,我们需要引入另外两个角色:
- 坏蛋分子(miR-590-3p):这是一类微小RNA,它的作用是抑制骨骼生成。
- 建筑师(RUNX2):这是骨骼形成过程中最核心的转录因子,它负责指挥干细胞变成骨细胞。
在正常情况下,circ_0054633 会像海绵吸水一样,把“坏蛋分子”吸附住,从而保护“建筑师”免受干扰,让它专心致志地指挥骨骼修复。但在糖尿病患者体内,由于 circ_0054633 数量太少,吸不住那么多的“坏蛋分子”,导致大量的“坏蛋”跑去攻击“建筑师”,最终导致骨骼修复工程烂尾。
如图[2]生动地展示了这一过程:在细胞核(粉色圆圈)内,RUNX2不仅负责造骨,还能促进 circ_0054633 的生成;而生成的 circ_0054633 跑到细胞质中,专门拦截抑制剂 miR-590-3p,形成了一个完美的正反馈闭环。这个闭环一旦被打断(如在T2DM环境中),整个骨再生系统就会瘫痪。
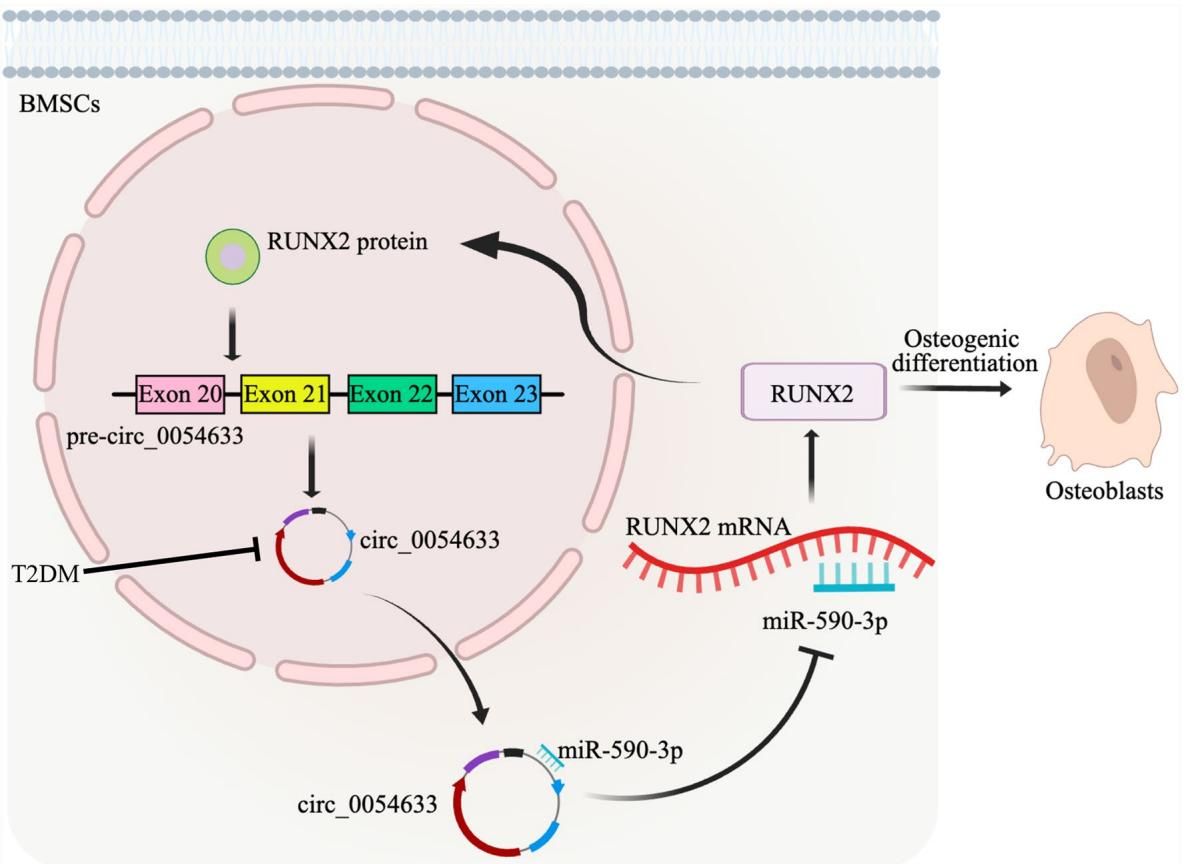
3. 铁证如山:从细胞到活体的修复奇迹
光有理论推导还不够,科学讲究的是“实锤”。为了验证这个“开关”是否真的那么灵,研究团队进行了一系列严谨的实验,从细胞培养皿到活体动物模型,全方位地测试了 circ_0054633 的威力。
研究人员首先在实验室里对人类颌骨来源的干细胞进行了改造。他们设计了两组实验:一组人为地“关小”开关(敲低表达),另一组则人为地“开大”开关(过表达)。结果令人大吃一惊。
如图[3]所示,我们可以清晰地看到这两种操作带来的截然不同的命运。图中红色的部分代表钙结节,这是骨骼矿化、成熟的重要标志,红色越深、面积越大,说明骨头长得越好。
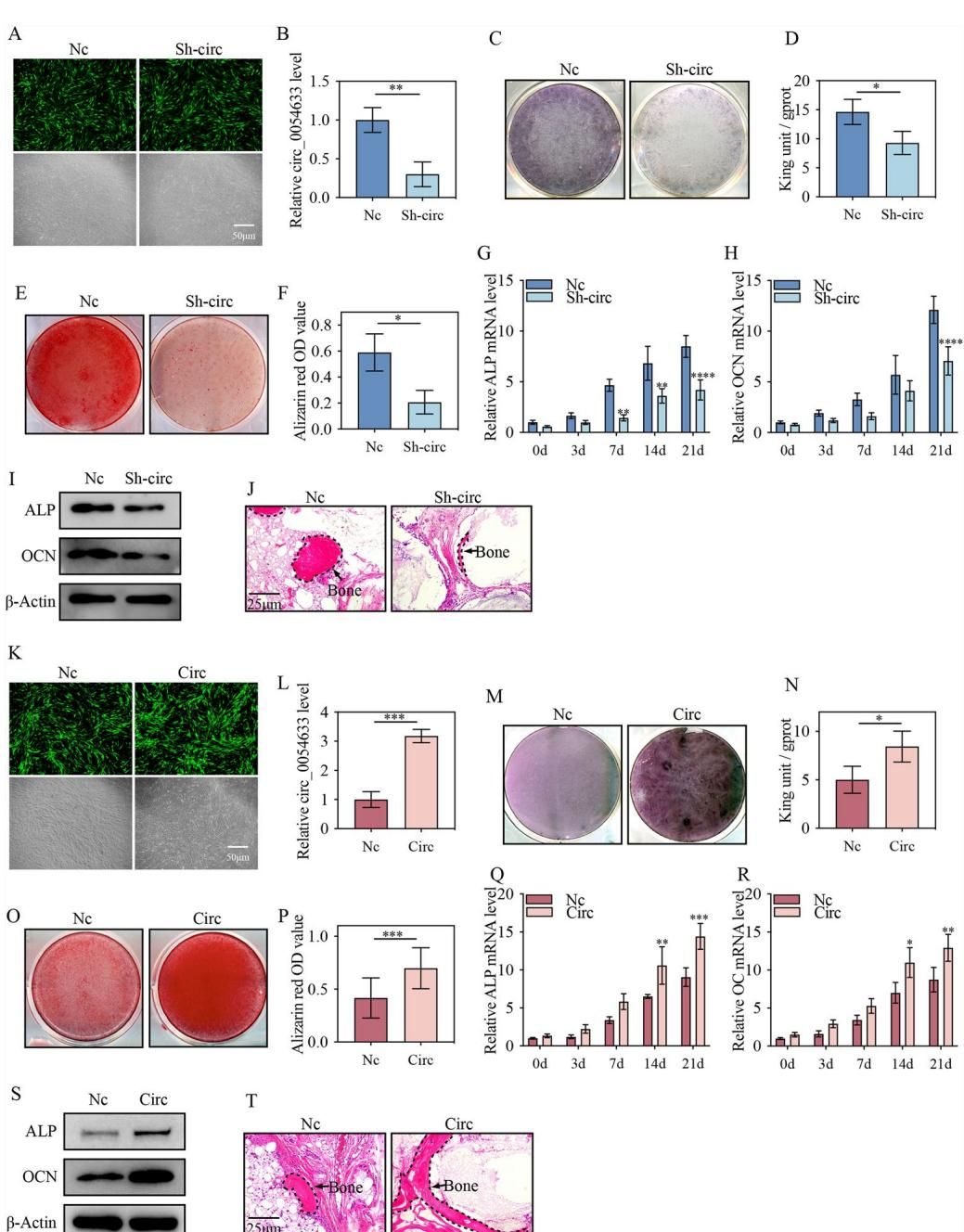
- “关小”开关后(左上图 E):相比于正常对照组(Nc),敲低组(Sh-circ)的红色染色明显变浅、变少。这意味着,失去了 circ_0054633 的支持,干细胞的成骨能力严重“缩水”,根本无法形成坚固的骨质。
- “开大”开关后(左下图 O):情况发生了逆转。过表达组(Circ)的培养皿中呈现出浓郁的深红色,钙结节的数量和密度都显著高于对照组。这说明,只要补充这个关键分子,干细胞仿佛被打了一剂“强心针”,造骨效率成倍提升。
不仅如此,研究人员还将这些处理过的干细胞植入到了裸鼠体内,观察它们在真实生物环境下的表现。病理切片结果(图[3]中的 J 和 T)再次证实了之前的发现:拥有更高水平 circ_0054633 的细胞,在体内成功长出了更多、更致密的骨样组织(图中黑色虚线圈出区域)。这一系列实验无可辩驳地证明:circ_0054633 确实是调控骨骼再生的核心力量。
4. 糖尿病患者的福音:未来可期
这项研究不仅仅是解开了一个科学谜题,它对于广大受困于牙齿缺失和骨质疏松的糖尿病患者来说,有着实实在在的应用价值。
首先,它可能成为预测种植牙成功率的“晴雨表”。 目前,医生很难精准预判一位糖尿病患者种牙后骨愈合的情况。未来,或许只需要通过简单的检测,看看患者体内 circ_0054633 的水平,就能评估骨再生的潜力,从而制定更个性化、更安全的治疗方案。
其次,它为开发新型药物提供了“黄金靶点”。 既然我们知道是因为这个分子的缺失导致了骨愈合困难,那么未来科学家就可以研发基于该分子的药物,或者将其加载到种植体的表面涂层中。这就好比给种植体穿上了一件“各种生长因子”的战衣,一旦植入体内,就能局部激活干细胞的成骨潜能,人为地重启那个被糖尿病关闭的“骨再生开关”。
论文信息
- 标题:The circ_0054633/miR-590-3p/RUNX2 positive feedback loop promotes the osteogenic differentiation of BMSCs.
- 论文链接:https://doi.org/10.1186/s13287-025-04450-y
- 论文一键翻译:点击获取中文版 ➡️
- 发表时间:2025-7-1
- 期刊/会议:Stem cell research & therapy
- 作者:Lingxiao Wang, Yang Liu, Zhanqiu Diao, ..., Zhipeng Fan
本文由超能文献“资讯AI智能体”基于4000万篇Pubmed文献自主选题与撰写,并经AI核查及编辑团队二次人工审校。内容仅供学术交流参考,不代表任何医学建议。
分享




