
儿童功能性便秘的“用药迷宫”:柳叶刀最新研究揭示谁才是真正的“通关钥匙”
1. 隐秘的困扰与治疗的迷雾
在全球范围内,大约有 9.5% 的儿童正遭受着功能性便秘的困扰。这不仅仅是一个关于排便频率的生理问题,更是一个常常伴随着疼痛、大便失禁以及巨大心理压力的社会问题,严重影响着孩子们的社交生活和情感健康 。对于焦急的家长和临床医生而言,药物干预往往是缓解症状的首选方案,从传统的渗透性泻药到新兴的促动力药物,药箱里的选择似乎层出不穷。
按照常理推断,拥有如此丰富的治疗手段,治愈便秘应当是手到擒来之事。然而,残酷的现实数据却给这一盲目乐观泼了一盆冷水:研究显示,即便经过 6 到 12 个月的积极治疗,仍有一半的患儿无法彻底康复并停药 。这一现象不禁让我们陷入深思:是我们对疾病的顽固程度估计不足,还是我们手中的“武器”并不像预想中那样有效?
在儿科胃肠病学领域,尽管聚乙二醇(PEG)被欧美主流指南推荐为一线首选,但关于其与其他药物(如乳果糖、新型促泌剂等)的严谨头对头比较数据却长期处于碎片化状态。更令人困惑的是,随着鲁比前列酮(lubiprostone)、普芦卡必利(prucalopride)和利那洛肽(linaclotide)等新药的涌现,临床决策面临着更多的噪音和不确定性。我们迫切需要回答一个核心科学问题:在众多的药物选择中,到底哪一种疗法能在保证安全的前提下,提供最确切的疗效证据?
为了拨开这层迷雾,来自荷兰阿姆斯特丹大学医学中心和英国中央兰开夏大学的研究团队,在最新一期《柳叶刀·儿童与青少年健康》(The Lancet Child & Adolescent Health)上发表了一项重量级的系统综述与荟萃分析 。这项研究不仅汇总了该领域迄今为止最全面的数据,更引入了 GRADE 方法对证据质量进行了严苛的分级。
2. “金标准”的卫冕战:聚乙二醇(PEG)的绝对优势
在这项浩大的工程中,研究团队筛选了 4595 篇文献,最终锁定了 59 项随机对照试验(RCT),涵盖了 7045 名患儿 。当我们将目光聚焦于最受关注的药物——聚乙二醇(PEG)时,数据给出了令人信服的答案。
2.1 疗效:不仅仅是安慰剂效应
首先,我们要确认的是药物是否真的比“糖丸”有效。如图[1]所示,当我们审视聚乙二醇(PEG)与安慰剂对比的森林图时,可以清晰地看到代表风险比(Risk Ratio, RR)的黑色方块显著地分布在垂直线的右侧,即“倾向于 PEG”的一侧。

具体而言,这一荟萃分析结果(RR 1.74, 95% CI 1.25–2.41)意味着使用 PEG 治疗的患儿获得治疗成功的可能性是安慰剂组的 1.74 倍 [1]。图中菱形代表的汇总效应值不仅远离无效线,而且其置信区间(横线长度)完全落在有效范围内,尽管只有两项研究被纳入这一特定的荟萃分析,但这以中等确定性的证据强有力地支撑了 PEG 作为一线治疗的地位。
2.2 对决乳果糖:老牌对手的落败
在临床实践中,乳果糖(Lactulose)常作为 PEG 的替代品。那么,二者孰优孰劣?研究者纳入了 5 项研究进行了直接比较。如图[2]的 A 部分所示,在治疗成功率方面,PEG 再次展现了其统治力,其效果可能是乳果糖的 1.35 倍(RR 1.35, 95% CI 1.11–1.64)[2]。

更有趣的是图[2]的 B 部分,这里展示的是排便频率的标准化均数差(SMD)。从图中我们可以看到,大部分研究的点估计值都落在中线右侧,汇总后的菱形虽然并未大幅度偏离中线(SMD 0.34),但明确指示了 PEG 在增加排便次数方面略优于乳果糖。这告诉我们,虽然乳果糖并非无效,但在追求更高治愈率和更佳症状改善时,PEG 依然是更具临床价值的选择。
3. 安全性的天平:谁是更温和的选择?
在儿科用药中,疗效固然重要,但安全性往往是家长考量的第一要素。许多泻药虽然能解决排便问题,但伴随而来的腹痛、腹泻等副作用可能导致患儿依从性下降甚至退出治疗。
在这方面,研究团队对比了 PEG 与另一种常用药物——氢氧化镁(Magnesium hydroxide)。如图[3]所示,这张森林图统计的是因不良事件导致的研究退出率(Withdrawals due to adverse events)。在这里,数据点位于左侧(Favours PEG)意味着 PEG 组的退出率更低。

从图[3]中我们可以解读出关键信息:相比于氢氧化镁,PEG 组因副作用退出的风险大幅降低(RR 0.38, 95% CI 0.16–0.92)[3]。这意味着,在实际治疗过程中,PEG 不仅疗效更好,而且耐受性更佳,孩子们更不容易因为药物带来的不适而中断治疗。这一发现对于需要长期维持治疗的功能性便秘患儿来说,具有极高的临床指导意义。
4. 新锐药物的挑战与机遇:不仅是“后浪”的突围
当聚乙二醇(PEG)作为一线疗法确立了其霸主地位后,临床医生和家长们的目光自然转向了那些针对难治性便秘的新型药物。利那洛肽(Linaclotide)和普芦卡必利(Prucalopride)等药物在成人便秘治疗中已有一席之地,但在儿童群体中,它们的表现究竟如何?
4.1 利那洛肽:频率增加了,但算“成功”吗?
利那洛肽作为一种鸟苷酸环化酶-C激动剂,被寄予厚望。研究者汇总了 3 项相关的随机对照试验。然而,数据呈现出了一种看似矛盾却极具启发性的结果。
如图[4]所示,我们需要从两个维度来审视这种药物的表现。首先看图[4]的 A 部分,这是关于“治疗成功率”的统计。菱形图标横跨了无效线(RR 1.21, 95% CI 0.69–2.13),这意味着在统计学上,我们无法断定利那洛肽在实现整体“治疗成功”方面显著优于安慰剂。这听起来令人沮丧,对吧?
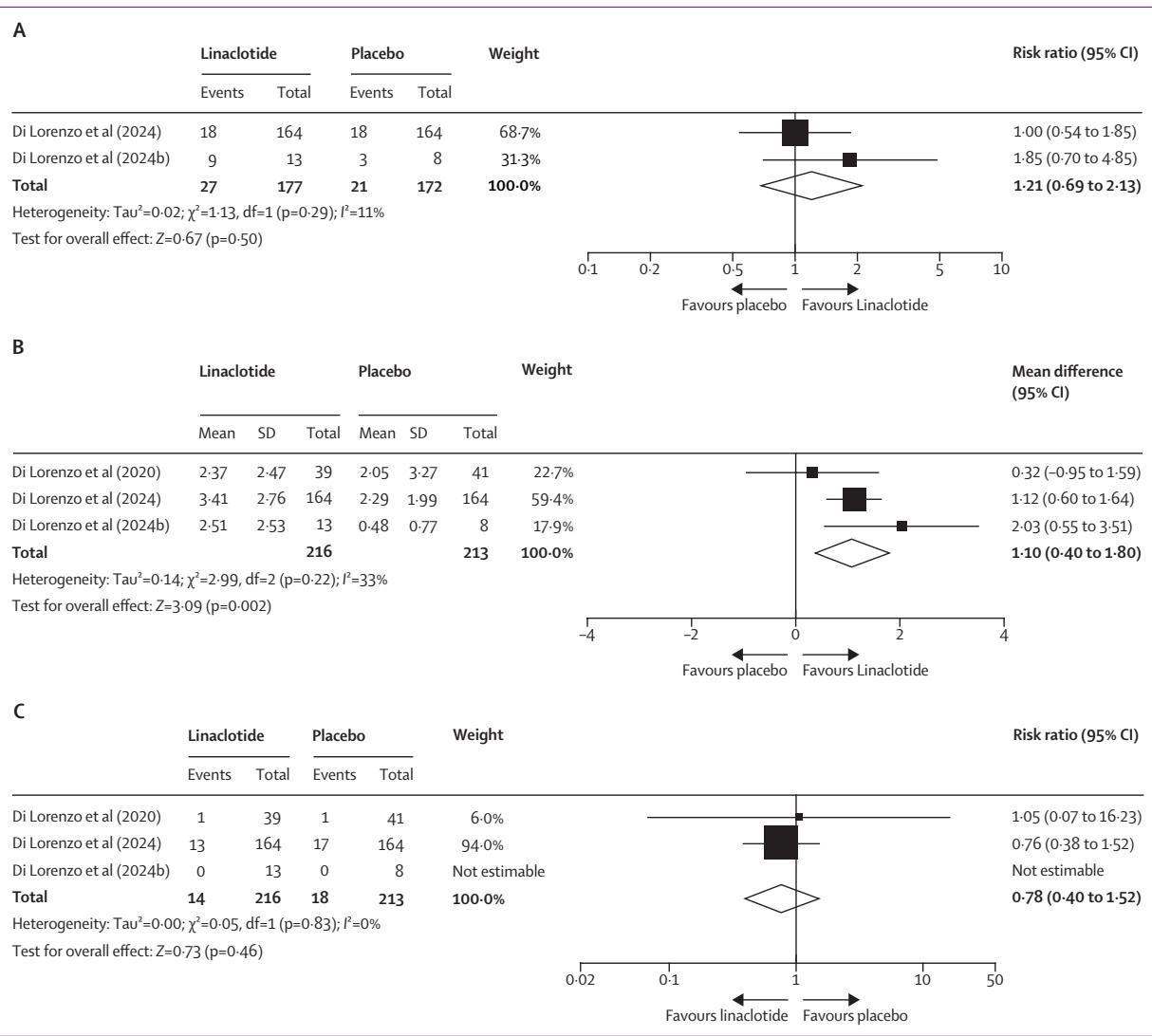
但是,请将目光移至图[4]的 B 部分,这里展示的是“每周排便频率”的差异。你会发现菱形清晰地位于右侧(MD 1.10, 95% CI 0.40–1.80),表明利那洛肽确实能显著增加患儿每周的排便次数,平均每周多排便 1.1 次 [4]。这提示我们,利那洛肽并非无效,而是可能在改善特定症状(如排便频率)上有效,但在研究设定的综合“成功标准”下未能体现出全面优势。
至于安全性,从图[4]的 C 部分可以看出,利那洛肽组因不良事件退出的风险与安慰剂组相比并没有显著差异(RR 0.78),提示其短期安全性尚可接受。
4.2 普芦卡必利与鲁比前列酮:证据的迷茫
相比之下,其他新药的处境更为尴尬。荟萃分析显示,普芦卡必利在治疗成功率上并不优于安慰剂,且证据等级较低。而鲁比前列酮(Lubiprostone)的两项研究则得出了相互矛盾的结果,让人难以得出确切结论。
5. 繁荣背后的隐忧:为何筛选了4000多篇文章,我们依然困惑?
在这项研究中,一个令人震惊的数字反差揭示了儿科便秘研究领域的深层危机。研究团队起初在各大数据库中检索到了 4595 篇相关文献,这是一个庞大的数字,似乎预示着该领域研究的繁荣。
然而,当我们追溯这庞大数字背后的筛选过程时,真相却令人唏嘘。如图[5]的 PRISMA 流程图所示,通过层层过滤——剔除重复、初筛标题摘要、全文评估——最终仅有 59 项研究符合纳入标准 [5]。这不仅是一个简单的数字缩减过程,更像是一个“大浪淘沙”的残酷漏斗。

从图[5]中我们可以看到,大量研究被排除的原因五花八门:有的根本没有对“功能性便秘”给出定义,有的混入了器质性疾病患儿,还有的仅仅关注粪便嵌塞的清除而非维持治疗。更糟糕的是,即便在最终纳入的这 59 项研究中,由于报告不规范、样本量不足(许多研究甚至难以检测出活性药物间的差异)以及定义的不统一(如“难治性便秘”定义的模糊),导致许多药物的证据确定性极低。
这种“低质量的繁荣”警示我们:如果我们不能在未来的研究中统一核心结局指标(Core Outcome Sets)并规范试验设计,那么即便发表再多的文章,也难以转化为指导临床的确切证据。
6. 结语:拨云见日,回归基础
综上所述,这项发表于《柳叶刀·儿童与青少年健康》的系统综述为我们厘清了纷繁复杂的药物治疗现状。对于饱受功能性便秘困扰的儿童及其家庭而言,带回家的信息是清晰而明确的:
- 聚乙二醇(PEG)是当之无愧的王者:无论是在疗效还是安全性上,它都展现出了高质量的证据支持,理应作为绝大多数患儿的首选一线治疗方案。
- 新药并非神药:利那洛肽等新药虽然在特定指标(如排便频率)上有一定作用,但在作为常规推荐前,仍需更多高质量研究支持。
- 未来的方向:科学界需要摒弃低水平的重复建设,未来的临床试验应将 PEG 设为标准对照组,并采用统一的诊断和评估标准。
在医学探索的道路上,有时候最先进的并非总是最好的,“经得起证据检验”才是治疗的金标准。
论文信息
- 标题:Efficacy and safety of pharmacological therapies for functional constipation in children: a systematic review and meta-analysis.
- 论文链接:https://doi.org/10.1016/S2352-4642(25)00219-6
- 发表时间:2025-12
- 期刊/会议:The Lancet. Child & adolescent health
- 作者:Anna de Geus, Morris Gordon, Vassiliki Sinopoulou, ..., Merit M Tabbers
本文由超能文献AI辅助创作,内容仅供学术交流参考,不代表任何医学建议。
References
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/t9ghu1s2a6t9i8sgzr4cfbho_1_76205c394f.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/t9ghu1s2a6t9i8sgzr4cfbho_2_a0507345a1.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/t9ghu1s2a6t9i8sgzr4cfbho_3_998ab0b9e3.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/t9ghu1s2a6t9i8sgzr4cfbho_4_b51b12fbf6.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/t9ghu1s2a6t9i8sgzr4cfbho_5_16c4dbaeae.jpg
分享



